肺炎球菌の微生物学的特徴
肺炎球菌はグラム陽性の双球菌で、学名 Streptococcus pneumoniaeである。通常の血液寒天培地(ヒツジ、ウサギ等の血液寒天培地)に発育し、α溶血性(不完全溶血=緑色調の溶血)を示す。コロニーは自己融解が進むと、中央がくぼんだ特徴的な形状をとる。
肺炎、敗血症、髄膜炎などの起炎菌となる強毒菌である。しかし乳幼児などでは鼻咽頭にも常在している。
菌体表面に莢膜と呼ばれる多糖体を有する菌体構造を持ち、これをもとにした血清型の区別で、現在90種類以上に分類されている。
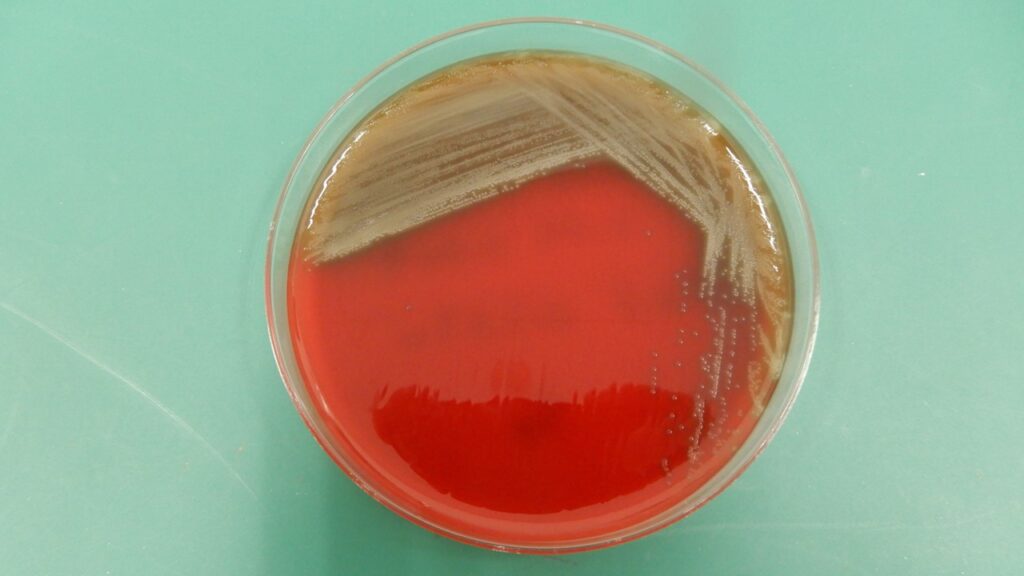
図 肺炎球菌のヒツジ血液寒天培地上の性状。α-溶血を示す。
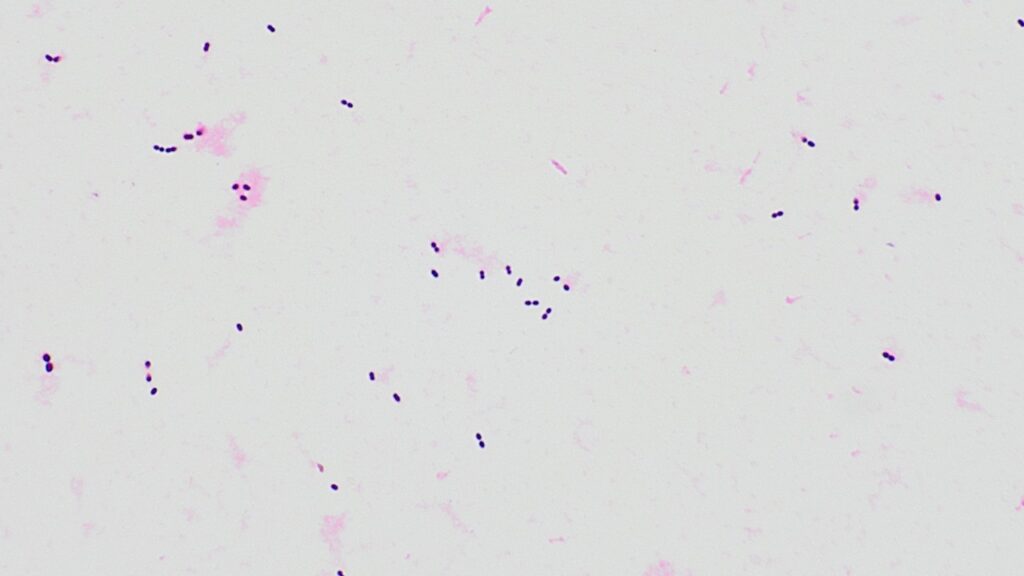
図 肺炎球菌のグラム染色.グラム陽性双球菌の形状を示す.
細菌性髄膜炎の診断、治療
細菌性髄膜炎の診療ガイドライン. 神経治療学会. pdf こちら.
年齢別の細菌性髄膜炎起因菌
周産期~生後1カ月まで
Group B Streptococcus (Streptococcus agalactiae), Escherichia coli, Listeria monocytogenes
生後1カ月~50歳まで
Streptococcus pneumoniae, Haemophilus influenzae (現在、小児へのHibワクチン定期接種導入により減少した),Neisseria meningitidis (アフリカ等の流行地~日本では散発的に発生)
50歳以上,アルコール多飲,細胞性免疫低下者
Streptococcus pneumoniae, Listeria monocytogenes, Gram陰性桿菌
成人の細菌性髄膜炎の一般的な治療
成人の髄膜炎は致死率が高く、かつ神経後遺症を残すことがあるため、初期に原因菌が判明していない症例では、
50歳未満では、
セフトリアキソンCTRX (またはセフォタキシムCTX)(ペニシリン耐性肺炎球菌、髄膜炎菌およびグラム陰性桿菌をカバーする)
+ バンコマイシンVCM(MRSA: メチシリン耐性黄色ブドウ球菌, PRSP: ペニシリン耐性およびセファロスポリン耐性肺炎球菌をカバーする)
+ ステロイド(デキサメサゾンは神経後遺症の予後を改善させる)
50歳以上、アルコール常飲、免疫不全者
ABPC(Listeria monocytogenesをカバーする)
+ CTRX (またはCTX)(同上)
+ VCM(同上)
+ステロイド(同上)
(これにアシクロビルACVを加えるかどうかは髄液の結果や総合判断による)
ペニシリン耐性肺炎球菌(penicillin-resistant Streptococcus pneumoniae:PRSP))出現の歴史
国立感染症研究所. こちら.
1967年頃、オーストラリアで、無γ-グロブリン血症の患者からペニシリンのMIC値が0.6μg/mlの肺炎球菌が報告された.
1974年、米国で化膿性髄膜炎の患者から、MIC値が0.25μg/mlの肺炎球菌が分離された。
1977年、現在のPRSPと同程度のペニシリン耐性 (MIC, 4μg/ml)を獲得した肺炎球菌が南アフリカのダーバンで分離された。
1970年代の後半より、この種のペニシリンに低感受性や耐性を示す肺炎球菌がスペイン、フランス、ドイツなどで徐々に問題となり始めた.
1980年代の後半には南米諸国やアジア各国からも分離されるようになった。 PRSPの血清型としては、6, 9, 14, 19, 23型が世界的に主流となっている。
1980年代の後半から欧米のみならず発展途上国などで増加し、現在、臨床分離される肺炎球菌の30~50%程度が PISP+PRSPと判定されるのが一般的となっている。
我が国でも、現時点で、PISP+PRSPの分離率が50%前後を示す医療施設が多くなってい る。喀痰、咽頭、鼻腔、耳漏などからの分離例が大半を占め、無症状のいわゆる「定着例」と考えられる事例も多い。
感染症における抗菌薬の治療の最小阻止濃度(MIC)とブレークポイント(break point)
薬剤感受性試験結果は、感染症治療に有用な抗菌薬の選択において有用な情報として提供する。投与される抗菌薬は、検査系内, in vitro における単なる最小発育阻止濃度(Minimum Inhibitory Concentration:MIC)を基に選択されるわけではなく,感染部位・臓器における抗菌薬濃度も加味して選択されなければならない。
薬剤感受性試験成績(特に最小阻止濃度, MIC)は、感染症の治療のために使われる抗菌薬を選択するための指標の一つにしか過ぎない。治療にあたって、薬剤感受性試験成績をどのように解釈して、適正な抗菌薬を選択するのかが重要である。しばしば感染症の治療において、「最も小さな値の最小発育阻止濃度を示す抗菌薬の治療効果が優れている」と考えられる傾向にあるが、治療効果は抗菌力(MIC)のみではなく、個々の薬物体内動態や組織内濃度(臓器到達性)が大きく影響する。これらを総合的に判断して抗菌薬を選択する。
抗菌薬選択は、薬剤感受性試験情報を基に、容易に抗菌薬を選択できるようにするためにブレイクポイントが考案された。ブレイクポイントは、in vitro の薬剤感受性検査結果から、抗菌薬の治療効果を予測するために使用する基準値である。CLSI のブレイクポイントは、感性(S) 、中間(I)および耐性(R)といった 3 種類の基準に分類されている。すなわち、対象菌株に感性と判定された抗菌薬は、対象菌株による感染症の治療にたいして臨床的効果が見込め、耐性と判定された場合には、治療ではその効果が見込めないことが想定される。
Clinical and Laboratory Standards Institute (CLSI) や European Committee on Antimicrobial Susceptibility Testing (EUCAST) は、ブレイクポイントを科学的根拠や臨床的根拠を基に毎年変更されている。
2008 年、CLSIは肺炎球菌に対するペニシリンGのブレイクポイントを変更した。(Clinical and Laboratory Standards Institute : Performance Standards for Antimicrobial Susceptibility
Testing; Eighteenth Informational Supplement. Vol.M100-S18. Wayne, Pennsylvania: CLSI, 2008)
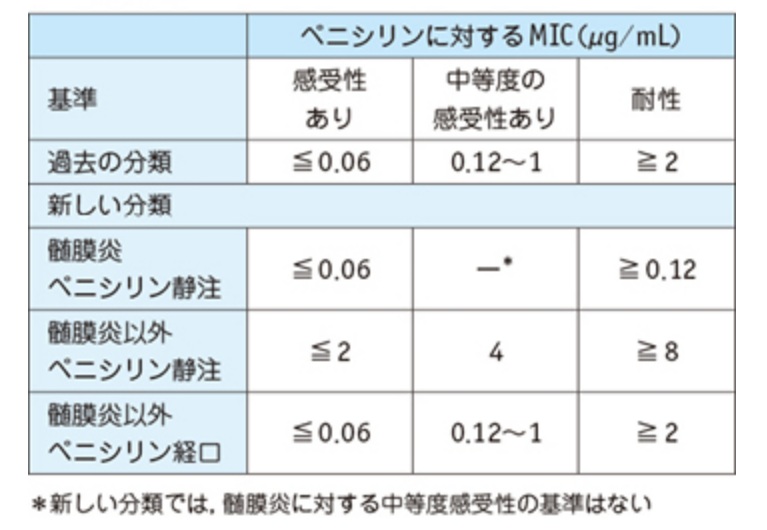
表. 肺炎球菌のペニシリンの最小阻止濃度MICのbreak pointsの変更. 関 雅文. こちら.
肺炎球菌のうち、ペニシリン耐性株(penicillin-resistant Streptococcus pneumoniae:PRSP)の定義が表の如く変更された.分離・同定された肺炎球菌のペニシリンGに対する最小発育阻止濃度(minimum inhibitory concentration:MIC)値が,微量液体稀釈法で,以前は一律に2 μg/mL以上の株とされていたが,肺炎など髄膜炎以外では,特に静注薬でのブレイクポイントとしては,8 μg/mL以上に変更された。
ペニシリン耐性肺炎球菌の耐性機序
初期のβ-ラクタム系薬であるペニシリンに由来して、これに耐性の菌株を「ペニシリン耐性肺炎球菌感染症」と呼ぶ。ペニシリン耐性肺炎球菌は、ペニシリンのみではなく、同時にセファロスポリン系薬の感受性も同時に低下している。これは類似するペニシリン結合蛋白の変異が関連しているためである。従ってペニシリン耐性肺炎球菌は、これに代替となる第3世代セファロスポリン系薬(セフトリアキソンやセフォタキシム)にも耐性となっており、髄膜炎治療におけるペニシリンおよびセファロスポリン系薬使用による失敗の可能性が高くなる。この場合治療薬はバンコマイシンおよび第3世代セファロスポリン系薬による治療が考慮される。
ペニシリン系薬やカルバペネム系薬は主にPBP1A,PBP2Bに強く作用・結合して菌を短時間で溶菌,殺菌性を発揮する。一方、セフェム系薬は主にPBP2Xに強く結合し、隔壁合成を阻害することによって抗菌力を発揮するとされる。菌が隔壁を有さずにに伸長化した後,細胞壁の脆弱部位から溶菌が起こるため,溶菌に至るまでにやや時間を要する(つまり、殺菌まで時間が掛かる)。
PRSPで同定されるPBP1A,PBP2X,そしてPBP2Bのアミノ酸配列の模式図を示す(図3)。黄色はPSSPのアミノ酸配列と異なったアミノ酸の置換が特に多く認められる領域である。それぞれのPBPをコードしているpbp1a,pbp2x,pbp2b遺伝子に変異が生じている。

図 肺炎球菌の薬剤耐性メカニズム. 重症型のレンサ球菌・肺炎球菌感染症に対するサーベイランスの構築と病因解析,その診断・治療に関する研究. こちら。
肺炎球菌のペニシリン耐性機序
β-ラクタム系薬耐性化には,菌の分裂・増殖に関わる細胞壁合成酵素(ペプチドグリカン架橋酵素)の機能的変化が関わっている。この酵素はβ-ラクタム系薬の作用標的であり,薬剤が結合すると細胞壁合成が阻害される。このため,penicillin-binding protein (PBP)と呼ばれる。
肺炎球菌には通常6種類のPBPが存在し,そのうち耐性に関わる主なPBPは,
- 細胞壁を長軸方向へ伸長化するPBP1A
- 隔壁合成を行なうPBP2X
- 本菌特有のランセット型形成に関わるPBP2B
の3種類が重要である。
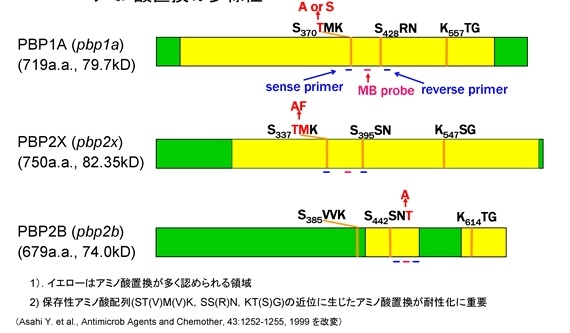
図 肺炎球菌の薬剤耐性メカニズム. 重症型のレンサ球菌・肺炎球菌感染症に対するサーベイランスの構築と病因解析,その診断・治療に関する研究. こちら。
ペニシリン系薬やカルバペネム系薬は主にPBP1A,PBP2Bに強く作用・結合して菌を短時間で溶菌,殺菌性を発揮する。一方、セフェム系薬は主にPBP2Xに強く結合し、隔壁合成を阻害することによって抗菌力を発揮するとされる。菌が隔壁を有さずにに伸長化した後,細胞壁の脆弱部位から溶菌が起こるため,溶菌に至るまでにやや時間を要する(つまり、殺菌まで時間が掛かる)。
PRSPで同定されるPBP1A,PBP2X,そしてPBP2Bのアミノ酸配列の模式図を示す(図3)。黄色はPSSPのアミノ酸配列と異なったアミノ酸の置換が特に多く認められる領域である。それぞれのPBPをコードしているpbp1a,pbp2x,pbp2b遺伝子に変異が生じている。
肺炎球菌におけるペニシリン耐性機序は、細胞壁架橋酵素であるペニシリン結合蛋白(PBP)の変異によるものである。ペニシリンを分解するペニシリナーゼ(またはβラクタマーゼ)は耐性機序には関与しない。よって肺炎球菌を含むStreptococcusの治療選択抗菌薬には、βラクタマーゼを含む抗菌薬(ABPC/SBT, PIPC/TAZ)は選択されない。
またβラクタマーゼを含む抗菌薬(ABPC/SBT, PIPC/TAZ)の髄液移行性は乏しく、髄膜炎を考慮した治療には選択できない。
ペニシリン耐性肺炎球菌、抗菌薬選択のまとめ
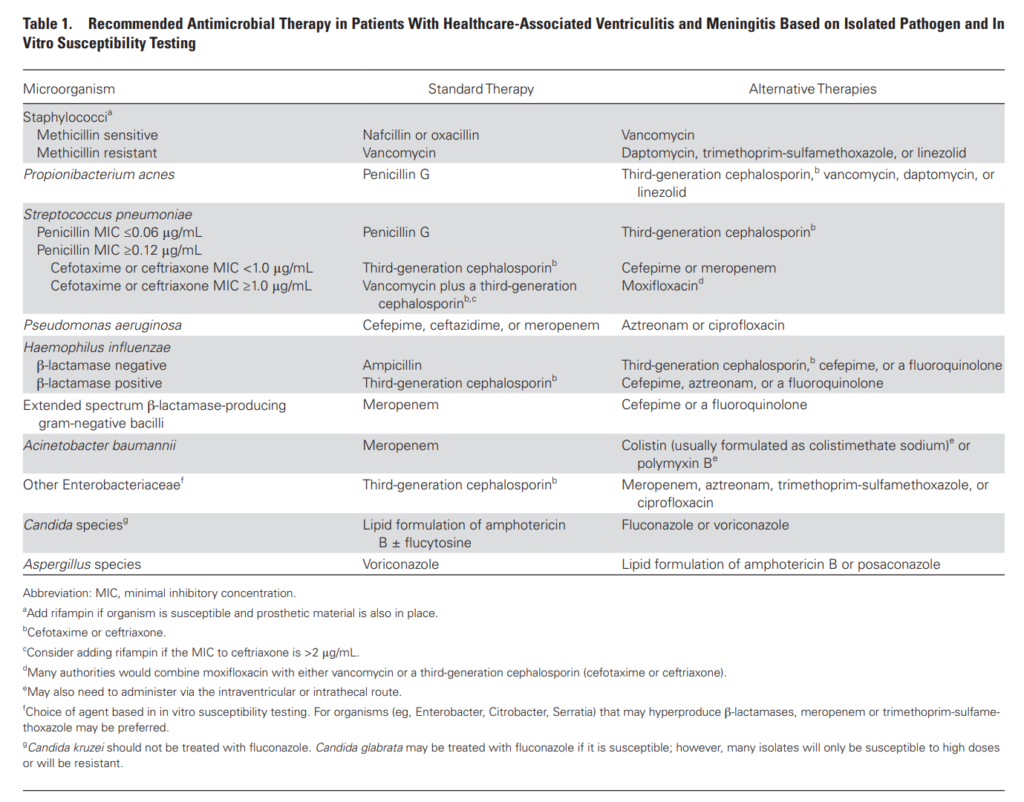
表 ペニシリン耐性肺炎球菌、抗菌薬選択. 2017 Infectious Diseases Society of America’s Clinical Practice Guidelines for Healthcare-Associated Ventriculitis and Meningitis. こちら.
肺炎球菌性髄膜炎の治療選択のまとめ
表の如く、肺炎球菌が確定され、かつ菌のMICが判明した後に、
ペニシリン感受性肺炎球菌PSSP:PCG のMIC<0.06であればPCGを選択する
ペニシリン耐性肺炎球菌PSSP、しかしセファロスポリン感受性肺炎球菌:PCG のMIC>0.12、しかしCTRXのMIC<1.0であれば、CTRX(またはCTX)を選択する。
ペニシリン耐性肺炎球菌PSSP、かつセファロスポリン耐性肺炎球菌:PCG のMIC>0.12かつCTRXのMIC>1.0であれば、VCM+CTRX(またはCTX)を選択する。



コメント