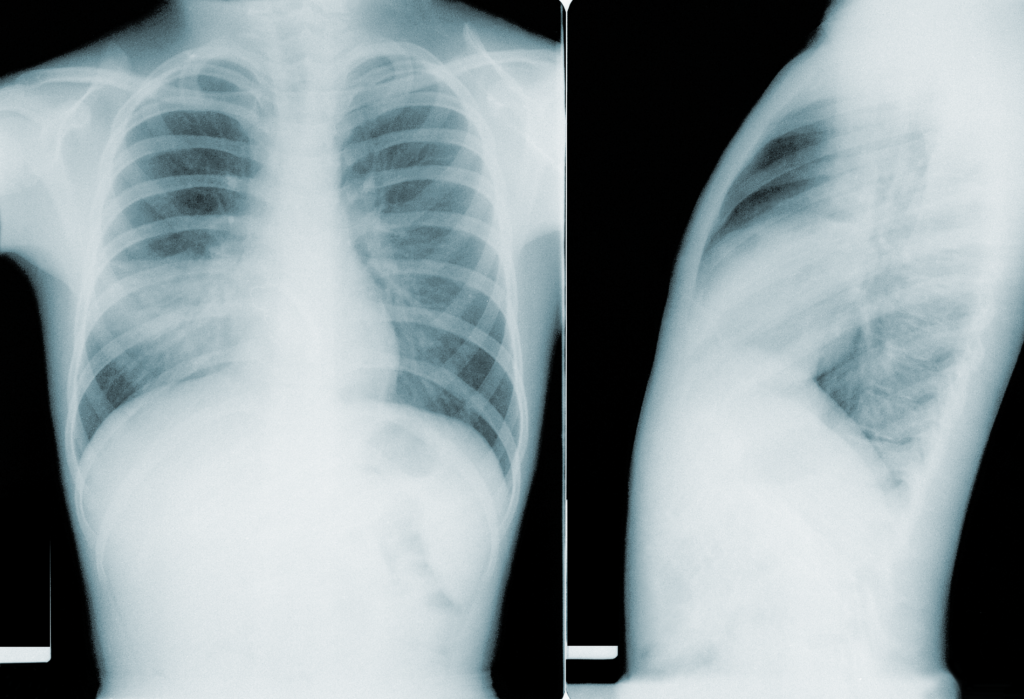
写真はマイコプラズマ肺炎の胸部X線像、CDC こちら。右肺炎。(写真向かって左が患者さんの右肺)
現在、マイコプラズマ・ニューモ二アエ(Mycoplasma pneumoniae)による肺炎が流行しています。
マイコプラズマ肺炎 8年ぶり大流行 感染気付かず広がるリスク NHK こちら。
Mycoplasma pneumoniaeとは
皿谷 健.マイコプラズマ肺炎.臨床と微生物 49(1): 39-43, 2022. こちら。一部編集して記載。
Mycoplasma pnemoniae (M. pneumoniae)(以下Mp)は細胞壁を持たない0.1~数 μmの大きさの細菌で,生きた細胞を含まない人工培地で自己増殖可能な最小の微生物である.非常に小さいため、通常の光学顕微鏡下のグラム染色では同定することはできない(見えない).比較として、大腸菌の大きさは約1~2 μm、ウイルスで最も小さなウイルスはパルボウイルスで、直径約20~25 nmである。
Mpの菌体および細胞侵入像、CDC こちら。
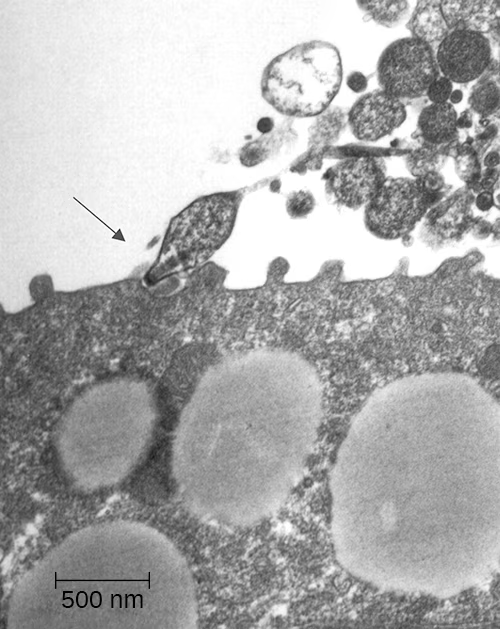
Mpの菌の内部構造、Mycoplasma pneumoniae: Current Knowledge on Macrolide Resistance and Treatment, こちら。矢印は細胞内に侵入しようとしているMp.
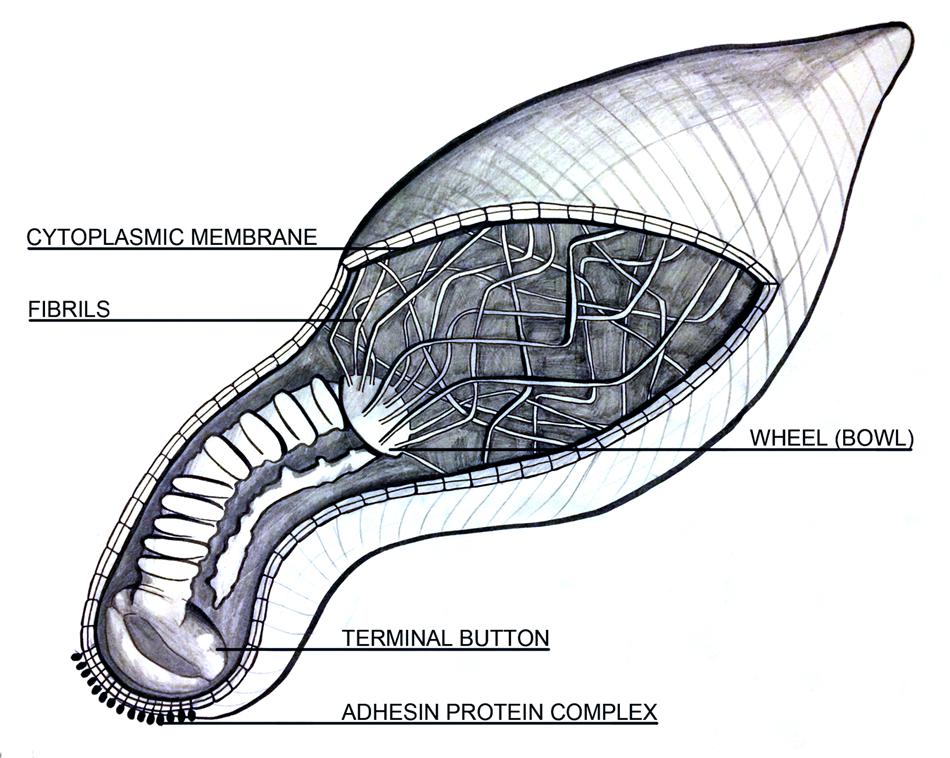
Mpの菌細胞の形状を示す。鞭毛は欠如、2つの分節板 (1 つは厚く、もう1方は薄い) で構成される。細胞質全体には線維があり、車輪様構造 (ボウル) 複合体などの特徴的な構造がある。
Mpは宿主の呼吸器気道上皮のP1蛋白質を介して接着し、感染が起こる。細胞に付着したMpから過酸化水素H2O2が産生され、気道上皮の障害が起こる。
Mycoplasma pneumoniae の病原性因子 国立感染症研究所、こちら。
M. pneumoniae はフラスコ型の突起部分、接着器官と呼ばれる接着に必要なタンパク質が集まった部位で呼吸器上皮細胞の繊毛に付着した後、滑走運動と呼ばれる運動で細胞表面に移動し、接着する。その接着・滑走運動に中心的な役割を果たしているのは、細胞表面に存在するP1アドヘジンと呼ばれるタンパク質、およびP30、P40、P65、P90、HMW1-3などのアクセサリータンパク質である.
Mp培養可能な培地
PPLO培地では目玉焼き(fried egg-appearance)のようにみえる.
菌種名の由来
Mpは、真菌様の形態を意味するmykes(fungus)とplasma(formed)というギリシヤ語に由来する.M. pneumonαeを鶏卵を用いて培養し種々の動物モデルで肺炎を作りあげたのはEaton博士である(1944年にEaton agent;Eatonが発見した病原体として報告された)。しかし菌を同定する技術がなかったこと(菌を同定できなかった),人体実験での再現性を確認しなかったため,長い間、ウイルスと考えられ、細菌として認識されていなかった。実際にMpが細菌であると認められたのは1963年である.
流行
マイコプラズマ肺炎は1981年4月から感染症発生動向調査が行われ,以前は4年ごとの流行が
ありオリンピック肺炎と名づけられたが,近年はその傾向は崩れ2006年,2010年,2011年,2012
年に患者数が増加している.2010~2013年には欧州各国でもマイコプラズマ肺炎の大きな増加が報告されている。
国立感染症研究所の定点当たりの報告数によれば,マイコプラズマ肺炎はコロナ禍の2020年以降は著明な減少を示している。
2015年から2023年までの報告。マイコプラズマ肺炎、12頁、こちら。
薬物耐性
Saraya. Novel aspects on the pathogenesis of Mycoplasma pneumoniae pneumonia and therapeutic implications. こちら。
本邦ではマイコプラズマ肺炎のマクロライド耐性が問題となっており,小児の60%以上,成人の30%以上がマクロライド耐性と考えられる.
マクロライド耐性 Mp は 2000 年以降に東アジアで出現し、拡大した。マクロライド耐性 Mp 分離株では 、23S rRNA (tRNA) のV領域の変異が多く報告されている。
これまでに 2063 位のアデニンがグアニンに置換された変異(A2063G と表記,以下同様)A2063C,A2063T,A2064G,C2617G の5 つの点変異が報告されている。
これらの変異は、エリスロマイシン、アジスロマイシン、クラリスロマイシンなどのマクロライドに対する最小発育阻止濃度の上昇と関連している。これまでの研究で、マクロライド耐性 Mp 肺炎患者は、小児と成人の両方で、マクロライド感受性 Mp 肺炎患者と比較して発熱が長引くとされている。マクロライド耐性 Mp 肺炎患者では、症状、検査結果、放射線学的所見、呼吸不全の合併症、死亡率などの臨床所見は、マクロライド感受性 Mp 肺炎患者と差はない。しかし、マクロライドの開始後 48 時間以上発熱が持続する場合は、マクロライド耐性 Mp の存在を示している可能性がある。
欧州での耐性菌流行
Macrolide-resistant Mycoplasma pneumoniae pneumonia in adolescents and adults: clinical findings, drug susceptibility, and therapeutic efficacy. こちら。
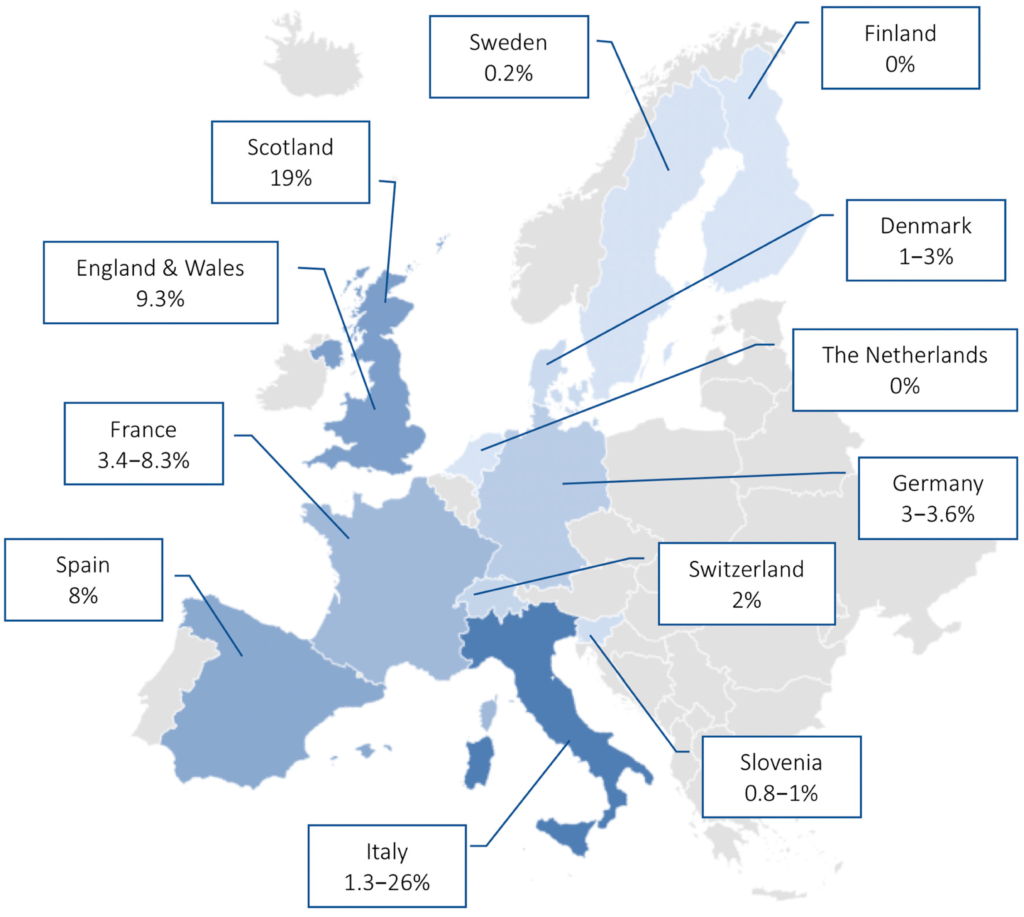
ヨーロッパでは比較的低い割合で、マクロライド耐性 Mp (MR-MP)の流行・拡散が報告されているた。ヨーロッパ、特に2010~2011年の流行中にMR-MP感染率が、最も高かったのはイタリアとスコットランドであった。対照的に、フィンランドとオランダではMR-MP感染は報告されなかった。
耐性菌、流行の図。
Mpのマクロライド耐性機序
Sabine Pereyre. Mycoplasma pneumoniae: Current Knowledge on Macrolide Resistance and Treatment こちら。
マクロライド系抗生物質は、細菌のリボソーム50Sサブユニットの23S rRNAに結合し、ペプチド転移反応を阻害することによりタンパク質合成を阻害し、抗菌作用を示す。
MiFuPでは、(1)23S rRNAのメチル化、(2)排出タンパク質による排出、(3)マクロライド分解酵素、および(4)マクロライド修飾酵素による不活性化が推測されている。
5S rRNA、16S rRNA、23S rRNAから構成されている。16S rRNAの30Sサブユニット上にはmRNAが結合し、23S rRNAの50Sサブユニット上にはtRNAによって運ばれ、アミノ酸からポリペプチド鎖が形成される。実際には23S rRNA遺伝子ドメインV領域の点変異の有無を調べる。
*ポリペプチド鎖のアミノ末端は、アミノ酸配列の変化が大きいことから、比較的変化の少ない定常領域 (C 領域) と区別するために可変領域 (ドメインV 領域) と呼ばれる。こちら。
下図は、Mpの 23S rRNA のドメイン V 領域のtRNAのループ構造を示す。四角で囲んだヌクレオチドは、in vitro 選択マクロライド耐性変異株で変異した位置を示す(in vitro株)。in vitro 選択に使用した抗生物質は括弧内に示す(14M:14 員環マクロライド:エリスロマイシンEM、クラリスロマイシンCAM、ロキシスロマイシンROXを含む、 15M:15 員環マクロライド:アジスロマイシンAZM、16M:16 員環マクロライド:ジョサマイシン、SC、ストレプトグラミンの組み合わせ、K、ケトライド)。丸で囲んだヌクレオチドは、臨床的なマクロライド耐性分離株(in vivo株)で変異した位置を示す。
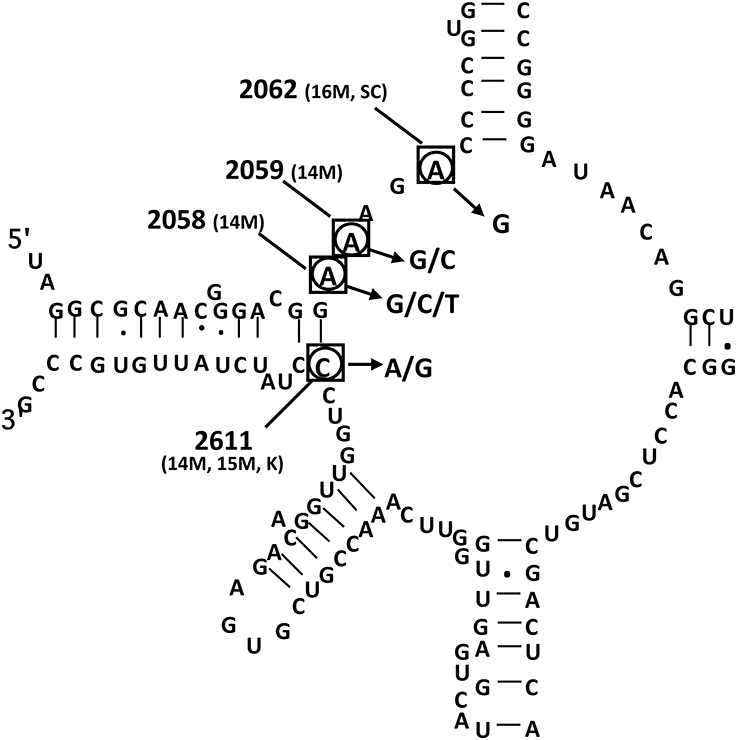
耐性株を想定した実際の治療
Mycoplasma pneumoniae: Current Knowledge on Macrolide Resistance and Treatment, こちら。
実際の医療現場では、Mp肺炎を疑って治療しても、これの耐性菌株同定することは容易ではない。初期治療において、マクロライド耐性Mpの可能性を否定できなくても、第一選択薬はマクロライドである。
マクロライドおよび関連抗生物質は、主に細菌に対する MIC が低く、毒性が低く、幼児に禁忌がないため、M. pneumoniae 呼吸器感染症の第一選択薬である。
第一選択薬は、ガイドラインや国ごとの流行状況、背景などで異なる。新型マクロライドに位置付けられるクラリスロマイシンCAMまたはアズスロマイシンAZMは、M. pneumoniae による市中肺炎の治療に、経口クラリスロマイシンを7~14 日間、または経口アジスロマイシンを5日間使用される。
適切な抗菌療法により、M. pneumoniae 感染症の症状期間は通常短縮され、放射線学的消失および回復が早まる。しかし、リアルタイム PCR を使用すると、M. pneumoniae DNA の保有期間の中央値は疾患発症後7週間である。つまり適切な抗菌薬治療を行っても患者検体(主に喀痰)中の Mp DNA 排泄の持続期間は短縮されないことがわかっている。肺外症状に対する治療に関する推奨事項はない。マクロライド系以外では、フルオロキノロン系、主にレボフロキサシンの治療効果が示されている。
肺炎マイコプラズマの実験室診断、国立感染症研究所、こちら。
Lampによる診断、栄研化学、pdf.
まとめ
Mycoplasma pneumoniae感染症の治療第一選択薬はマクロライド.投与後48時間経過して解熱しなければマクロライド耐性を疑う。この場合は、フルオロキノロン系(レボフロキサシンなど)、テトラサイクリン系(ミノサイクリン)が選択されることがある。
鈴木 裕、薬剤耐性肺炎マイコプラズマの分子疫学、こちら。
冒頭の写真は、袋田の滝、こちら。



コメント